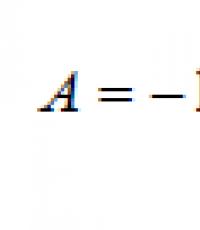Propriétés physicochimiques de l'oxyde de zinc. Oxyde de zinc: propriétés, préparation et application
Vues détaillées: 9373
Zinc blanc
Oxyde de zinc.
Formule chimique du produit: ZnO
Désignations commerciales des produits:
- Zinc blanc
- Zinc blanc
- Oxyde de zinc
- Fleurs de zinc
- C.I. pigment blanc 4
- Oxozinc
- Zincite
- Pâte de Lassar
Description du produit:
Oxyde de zinc est un composé inorganique de formule ZnO. Oxyde de zinc est une poudre blanche insoluble dans l'eau et largement utilisée comme additif dans de nombreux matériaux et produits, y compris les caoutchoucs, les plastiques, la céramique, le verre, le ciment, les lubrifiants, les peintures, les onguents, les adhésifs, les mastics, les pigments, les aliments, les batteries, les ferrites , ignifuges et du scotch. Bien qu'il se produise naturellement comme le zinc minéral, la plupart oxyde de zinc obtenu par synthèse. Zinc blanc est un semi-conducteur à large gap du groupe des semi-conducteurs II-VI. Dopage naturel d'un semi-conducteur en raison de lacunes d'oxygène ou d'interstices de zinc de type n. Ce semi-conducteur a un certain nombre de propriétés favorables, notamment une bonne transparence, une mobilité électronique élevée, une large bande interdite et une forte luminescence à température ambiante. Ces propriétés sont précieuses dans de nouvelles applications pour: les électrodes transparentes dans les écrans à cristaux liquides, les fenêtres d'économie d'énergie ou de protection thermique, et l'électronique sous forme de transistors à couches minces et de diodes électroluminescentes. Oxyde de zinc (aussi appelé zinc blanc) est une poudre amorphe blanche ou jaunâtre, insoluble dans l'eau et l'alcool, mais soluble dans acide et alcalis... Particules oxyde de zinc peut être sphérique, en forme d'aiguille ou sphérique selon le processus de fabrication. La forme des particules est importante pour maximiser les propriétés physiques. Oxyde de zinc absorbe pratiquement tous les rayons ultraviolets inférieurs à 360 nm et offre une excellente protection du liant. Oxyde de zinc réagit avec les composants acides des revêtements et forme savons de zinc. Savons de zinc améliorer la flexibilité et la dureté des revêtements. Il est utilisé comme pigment dans la formulation de caoutchouc, comme pigment blanc dans l'industrie céramique, comme base opaque dans les cosmétiques et a d'autres utilisations dans les industries du papier, de la peinture et du verre optique.
Oxyde de zinc cristallise sous deux formes principales: wurtzite hexagonale et blende galvanisée cubique. La structure wurtzite est la plus stable dans les conditions ambiantes et donc la plus abondante. La forme de la blende de zinc peut être stabilisée en faisant croître de l'oxyde de zinc sur des substrats à structure en treillis cubique. Dans les deux cas, les centres du zinc et de l'oxyde sont tétraédriques, la géométrie la plus caractéristique du Zn (II). Oxyde de zinc se transforme à des pressions relativement élevées, environ 10 GPa. Les polymorphes hexagonaux et galvanisés n'ont pas de symétrie d'inversion (la réflexion du cristal par rapport à un point donné ne le transforme pas en lui-même). Ceci et d'autres propriétés de la symétrie du réseau conduisent à la piézoélectricité de l'oxyde de zinc hexagonal et galvanisé et à la pyroélectricité de l'oxyde de zinc hexagonal. Comme avec la plupart des matériaux du groupe II-VI, la liaison des structures atomiques dans l'oxyde de zinc est largement ionique (Zn 2 + -O 2 -) avec des rayons correspondants de 0,074 nm pour Zn2 + et 0,140 nm pour O 2 -. Cette propriété explique la formation prédominante de la structure wurtzite plutôt que de la blende de zinc, ainsi que la forte piézoélectricité oxyde de zincet. En raison des liaisons polaires Zn-O, les plans de zinc et d'oxygène sont chargés électriquement. Pour maintenir l'électroneutralité, ces plans sont restaurés au niveau atomique dans la plupart des matériaux relatifs, mais pas dans oxyde de zinc - ses surfaces sont atomiquement planes, stables et n'ont pas de reconstruction. Cette anomalie oxyde de zinc pas entièrement expliqué.
Oxyde de zinc - un matériau relativement mou d'une dureté approximative de 4,5 sur l'échelle de Mohs. Ses constantes élastiques sont inférieures à celles des semi-conducteurs III-V correspondants tels que GaN. Capacité thermique et conductivité thermique élevées, faible dilatation thermique et point de fusion élevé oxyde de zinc bénéfique pour la céramique. Parmi les semi-conducteurs à couplage tétraédrique, il a été déclaré que oxyde de zinc a le tenseur piézoélectrique le plus élevé ou au moins comparable à GaN et AlN. Cette propriété en fait un matériau technologiquement important pour de nombreuses applications piézoélectriques qui nécessitent une connexion électromécanique importante. Oxyde de zinc a une bande interdite avant relativement grande de ~ 3,3 eV à température ambiante. Les avantages associés à un écart de plage plus large comprennent des tensions de claquage plus élevées, la capacité de résister à des champs électriques importants, un bruit électronique plus faible et un fonctionnement à des températures et une puissance élevées. Écart oxyde de zinc peut être en outre réglé à ~ 3-4 eV en le dopant avec de l'oxyde de magnésium ou de l'oxyde de cadmium. Plus oxyde de zinc a un caractère de type n, même en l'absence d'alliage délibéré. La non-stoechiométrie est généralement la source du caractère de type n, mais le sujet reste controversé. Une autre explication, basée sur des calculs théoriques, a été proposée selon laquelle les impuretés de déplacement d'hydrogène non intentionnelles en sont la cause. Un dopage de type n contrôlé est facilement obtenu en remplaçant Zn par des éléments du groupe III tels que Al, Ga, In, ou en remplaçant l'oxygène par des éléments du groupe VII par du chlore ou de l'iode.
En production oxyde de zincil existe trois méthodes principales.
- Méthode indirecte... Dans un processus indirect ou français métal de zinc fond dans un creuset en graphite et s'évapore à des températures supérieures à 907 ° C (généralement autour de 1000 ° C). Des couples zincréagissent avec l'oxygène de l'air, ce qui conduit à la formation de ZnO, accompagnée d'une baisse de sa température et d'une brillante luminescence. Particules oxyde de zinc transporté vers le canal de refroidissement et recueilli dans un sac. Cette méthode indirecte a été popularisée par LeClaire (France) en 1844 et est donc largement connue sous le nom de procédé français. Son produit est généralement constitué de particules agglomérées oxyde de zinc avec une taille moyenne de 0,1 à plusieurs micromètres. La plupart en poids oxyde de zinc produit dans le monde selon la méthode française.
- Processus direct... Le processus direct ou américain commence avec une variété de composites de zinc contaminés tels que minerais de zinc ou sous-produits du four de fusion. Précurseurs zinc réduit (réduction carbothermique) par chauffage avec une source de carbone telle que l'anthracite pour produire des vapeurs zinca, qui est ensuite oxydé, comme dans le cas d'un procédé indirect. En raison de la plus faible pureté du matériau de départ, le produit final a également une qualité inférieure dans le processus direct par rapport au produit indirect.
- Procédé chimique humide ... Une petite quantité de production industrielle est associée à des processus chimiques par voie humide qui commencent par des solutions aqueuses de sels de zinc à partir desquelles précipitent carbonate de zinc ou hydroxyde de zinc... Le précipité solide est ensuite calciné à des températures d'environ 800 ° C.
Il existe de nombreuses méthodes spécialisées pour obtenir oxyde de zinc pour la recherche et le développement et les applications de niche. Ces méthodes peuvent être classées selon la forme obtenue de ZnO (en vrac, couche mince, nanofil), la température («faible», proche de la température ambiante ou «élevée», c'est-à-dire T ~ 1000 ° C), le type de procédé (dépôt en phase vapeur ou croissance à partir d'une solution) et d'autres paramètres. De grands monocristaux (plusieurs centimètres cubes) peuvent être développés par transfert de gaz (dépôt en phase vapeur), synthèse hydrothermale ou croissance en fusion. Cependant, en raison de la pression de vapeur élevée oxyde de zinc la croissance en fusion est problématique. Il est difficile de contrôler la croissance du transport de gaz, laissant la méthode hydrothermale en faveur. Des films minces peuvent être produits par dépôt chimique en phase vapeur, épitaxie en phase vapeur à structure métallique, électrodéposition, dépôt laser pulsé, pulvérisation, synthèse sol-gel, dépôt de couche atomique, pyrolyse par pulvérisation, etc. Poudre blanche ordinaire oxyde de zinc peut être obtenu en laboratoire par électrolyse d'une solution de bicarbonate de sodium avec une anode en zinc. Fabriqué hydroxyde de zinc et l'hydrogène. Hydroxyde de zinc se décompose en oxyde de zinc lorsqu'il est chauffé. Les nanostructures d'oxyde de zinc peuvent être synthétisées dans une variété de morphologies, y compris les nanofils, les nanorods, les tétrapodes, les nanoobjets, les nanofibres, les nanoparticules, etc. Les nanostructures peuvent être obtenues en utilisant la plupart des méthodes ci-dessus dans certaines conditions, ainsi qu'en utilisant la méthode vapeur-liquide-solide. La synthèse est généralement effectuée à des températures d'environ 90 ° C dans une solution aqueuse équimolaire de nitrate zinca et hexamine, cette dernière fournissant le milieu basique. Certains additifs tels que le polyéthylène glycol ou la polyéthylèneimine peuvent améliorer le rapport de taille des nanofils oxyde de zinc... Dopage des nanofils oxyde de zinc a été obtenu en ajoutant d'autres nitrates métalliques à la solution de croissance. La morphologie des nanostructures résultantes peut être réglée en modifiant les paramètres liés à la composition des précurseurs (tels que la concentration de zinc et le pH) ou au traitement thermique (tels que la température et la vitesse de chauffage).
Propriétés physicochimiques Oxyde de zinc.
|
indicateurs |
valeur |
|
|
Condition physique et apparence oxyde de zinc |
Solide (poudre solide) |
|
|
Odeur oxyde de zinc |
Sans odeur |
|
|
Goût oxyde de zinc |
Amer |
|
|
Masse moléculaire oxyde de zinc |
81,38 g / mol |
|
|
Couleur oxyde de zinc |
blanc à blanc jaunâtre |
|
|
La température de fusion oxyde de zinc |
1975 ° C (3587 ° F) |
|
|
Gravité spécifique oxyde de zinc |
5,607 (eau \u003d 1) |
|
|
Propriétés de dispersion oxyde de zinc |
Non dispersible dans l'eau froide, l'eau chaude. |
|
|
Solubilité oxyde de zinc |
Ne se dissout pas dans l'eau froide, l'eau chaude. Dissolvons dans de l'acide acétique dilué ou des acides minéraux, de l'ammoniaque, du carbonate d'ammonium, un alcali fixe. |
|
|
Stabilité oxyde de zinc |
stable |
Stockage et transport de l'oxyde de zinc:
Précautions:
Gardez fermé. Ne pas avaler. Ne respirez pas la poussière. Portez des vêtements de protection appropriés. En cas de ventilation insuffisante, porter un appareil respiratoire approprié. En cas d'ingestion, consulter immédiatement un médecin et lui montrer l'emballage ou l'étiquette. Tenir à l'écart des substances incompatibles telles que les acides.
Stockage: Garder le récipient bien fermé. Stocker le contenant dans un endroit frais et bien ventilé. Ne pas conserver à des températures supérieures à 25 ° C (77 ° F).
Applications d'oxyde de zinc:
- Applications de poudre oxyde de zinc sont nombreux et les principaux sont énumérés ci-dessous. La plupart des applications utilisent la réactivité de l'oxyde comme précurseur d'autres composés du zinc. Pour les applications en science des matériaux oxyde de zinc possède un indice de réfraction élevé, une conductivité thermique élevée, des propriétés liantes, antibactériennes et protectrices contre les UV. Par conséquent, il est ajouté aux matériaux et produits, y compris les plastiques, la céramique, le verre, le ciment, le caoutchouc, les lubrifiants, les peintures, les pommades, les adhésifs, les mastics, la production de béton, les pigments, les produits alimentaires, les batteries, les ferrites.
- Production de caoutchouc. L'industrie du caoutchouc utilise 50% à 60% oxyde de zinc. Oxyde de zinc avec l'acide stéarique utilisé pour la vulcanisation de l'additif en caoutchouc oxyde de zinc protège également le caoutchouc des champignons et des rayons ultraviolets.
- Industrie céramique. L'industrie céramique consomme une quantité importante oxyde de zinc, en particulier, dans les compositions de glaçure céramique et de fritte.La capacité thermique, la conductivité thermique et la stabilité à haute température relativement élevées de l'oxyde de zinc, combinées à un coefficient de dilatation relativement faible, sont des propriétés souhaitables dans la fabrication de céramiques.Oxyde de zinc affecte le point de fusion et les propriétés optiques des émaux, des émaux et des céramiques.Oxyde de zinc sous forme de faible dilatation, l'écoulement secondaire améliore l'élasticité des glaçures, réduit le changement de viscosité avec la température et empêche la fissuration.
- Médicament. Oxyde de zinc Il est largement utilisé pour traiter diverses affections cutanées, notamment la dermatite, les démangeaisons dues à l'eczéma, les couches et l'acné. Il est utilisé dans des produits tels que la poudre pour bébé et les crèmes protectrices pour les couches, les crèmes à la calamine, les shampooings antipelliculaires et les onguents antiseptiques. ... Oxyde de zinc peut être utilisé dans les onguents, les crèmes et les lotions pour protéger contre les coups de soleil et autres dommages cutanés causés par la lumière ultraviolette. De nombreux écrans solaires utilisent des nanoparticules oxyde de zinc (avec les nanoparticules le dioxyde de titane), car ces petites particules ne diffusent pas la lumière et n'apparaissent donc pas blanches. Nanoparticules oxyde de zinc peut améliorer l'activité antibactérienne de la ciprofloxacine.
- L'industrie du tabac. Oxyde de zinc fait partie intégrante des filtres à cigarettes. Le filtre, qui se compose de charbon imprégné d'oxyde de zinc et d'oxyde de fer, élimine des quantités importantes de cyanure d'hydrogène et de sulfure d'hydrogène de la fumée de tabac sans affecter son arôme.
- Complément alimentaire. Oxyde de zinc ajouté à de nombreux aliments, y compris les céréales pour petit-déjeuner, comme source de zinc, un nutriment essentiel. Sulfate de zinc également utilisé dans le même but.
- Production de pigments. Oxyde de zinc le blanc est utilisé comme pigment dans les peintures et est plus opaque que le lithopone mais moins opaque que le dioxyde de titane Il est également utilisé dans les revêtements de papier. Le blanc chinois est une qualité spéciale de blanc de zinc qui est utilisée dans les pigments des peintres. L'utilisation du zinc blanc (oxyde de zinc) comme pigment dans la peinture à l'huile a commencé au milieu du 18e siècle. Il a partiellement remplacé la plomb blanche toxique et a été utilisé par des artistes tels que Becklin, Van Gogh, Manet, Munch. C'est également l'ingrédient principal du maquillage minéral.
- Revêtements. Peintures en poudre oxyde de zincont longtemps été utilisés comme revêtements anticorrosion pour les métaux. Ils sont particulièrement efficaces sur le fer galvanisé. Le fer est difficile à protéger car sa réactivité avec les revêtements organiques se traduit par une fragilité et un manque d'adhérence. Peintures à base oxyde de zincconservent leur souplesse et leur adhérence sur de telles surfaces pendant de nombreuses années. Les plastiques tels que le polyéthylène naphtalate (PEN) peuvent être protégés avec des revêtements d'oxyde de zinc. Le revêtement réduit la diffusion d'oxygène avec PEN. Les couches d'oxyde de zinc peuvent également être utilisées sur les applications extérieures en polycarbonate (PC). Le revêtement protège le PC du rayonnement solaire et réduit le taux d'oxydation et le photo-jaunissement du PC.
- Prévention de la corrosion dans les réacteurs nucléaires ... Oxyde de zinc, appauvri en 64 Zn (un isotope du zinc avec une masse atomique de 64), est utilisé pour empêcher la corrosion dans les réacteurs à eau sous pression. L'épuisement est nécessaire car le 64 Zn est converti en 65 Zn radioactif lorsqu'il est irradié avec des neutrons du réacteur.
- Réforme du méthane . Oxyde de zinc est utilisé comme étape de prétraitement pour éliminer le sulfure d'hydrogène du gaz naturel après l'hydrogénation de tout composé soufré avant un reformeur de méthane qui peut empoisonner le catalyseur.
Formule structurelle
Nom russe
Nom latin de la substance Oxyde de zinc
Zinci oxydum ( genre. Zinci oxydi)Formule brute
ZnOGroupe pharmacologique de la substance Oxyde de zinc
Classification nosologique (CIM-10)
Code CAS
1314-13-2Caractéristiques de la substance Oxyde de zinc
Agent anti-inflammatoire topique. Blanc ou blanc avec un éclat jaunâtre, poudre amorphe et inodore. Absorbe le dioxyde de carbone de l'air. Pratiquement insoluble dans l'eau et l'éthanol, soluble dans les acides minéraux dilués et l'acide acétique, dans les solutions alcalines.
Pharmacologie
effet pharmacologique - antiseptique, astringent, asséchant.Forme des albumines et dénature les protéines. Lorsqu'il est appliqué sur la surface de la peau affectée, il réduit la gravité des processus exsudatifs, élimine les manifestations locales d'inflammation et d'irritation; a un effet absorbant, forme un revêtement protecteur sur la peau, ce qui réduit l'effet des facteurs irritants sur celle-ci. Appliquer extérieurement sous forme de poudre, pommade, pâte, liniment.
Application de la substance Oxyde de zinc
Dermatite, y compris la dermatite des couches (traitement et prévention), érythème fessier, chaleur épineuse; plaies et brûlures superficielles (y compris coups de soleil, coupures, égratignures), lésions cutanées ulcéreuses (y compris ulcères trophiques), escarres; eczéma au stade aigu, herpès simplex, streptodermie.
Contre-indications
Hypersensibilité.
Voie d'administration
Extérieurement.
Précautions pour la substance Oxyde de zinc
Éviter le contact visuel.
Interactions avec d'autres ingrédients actifs
Appellations commerciales
| Nom | Valeur de l'indice Vyshkovsky ® |
Ministère de l'éducation et des sciences de la Fédération de Russie
établissement d'enseignement budgétaire de l'État fédéral
enseignement professionnel supérieur
UNIVERSITÉ D'ÉTAT DE PETROZAVOD
faculté de médecine
Résumé sur la discipline "Chimie pharmaceutique"
Sujet: Oxyde de zinc. Sulfate de zinc.
Le travail a été réalisé par un étudiant du cours IV
Spécialité: pharmacie
Service de correspondance
Groupe: 73Z42
Rigoeva Anna Sergeevna
Vérifié le travail
Prof:
Ermakova Galina Vladimirovna
Petrozavodsk 2012
Le zinc est un élément d'un sous-groupe secondaire du deuxième groupe, la quatrième période du système périodique des éléments chimiques de D.I. Mendeleev, de numéro atomique 30.
Il est désigné par le symbole Zn (latin Zincum).
Le zinc, substance simple dans des conditions normales, est un métal de transition fragile de couleur blanc bleuâtre (il se ternit à l'air et se recouvre d'une fine couche d'oxyde de zinc).
Un exemple typique d'un métal formant des composés amphotères. Les composés de zinc ZnO et Zn (OH) 2 sont amphotères. Le potentiel d'électrode standard est de -0,76 V, dans la série de potentiels standard, il est situé avant le fer.
Dans l'air, le zinc est recouvert d'une fine pellicule d'oxyde de ZnO. Lorsqu'il est chauffé fortement, il brûle pour former de l'oxyde blanc amphotère ZnO:
L'oxyde de zinc réagit avec les solutions acides:
et alcalis:
Le zinc de pureté normale réagit activement avec les solutions acides:
et solutions alcalines: formation d'hydroxyzincates. Le zinc très pur ne réagit pas avec les solutions d'acides et d'alcalis. L'interaction commence par l'ajout de quelques gouttes d'une solution de sulfate de cuivre CuSO4.
Lorsqu'il est chauffé, le zinc réagit avec les halogènes pour former des halogénures de ZnHal2. Avec le phosphore, le zinc forme des phosphures Zn3P2 et ZnP2. Avec le soufre et ses analogues - sélénium et tellure - divers chalcogénures, ZnS, ZnSe, ZnSe2 et ZnTe.
Le zinc ne réagit pas directement avec l'hydrogène, l'azote, le carbone, le silicium et le bore. Le nitrure de Zn3N2 est produit par la réaction du zinc avec de l'ammoniac à 550-600 ° C.
Dans les solutions aqueuses, les ions zinc Zn2 + forment des complexes aqueux 2+ et 2+.
sulfate de zinc
ZnSO4, cristaux incolores. Se dissout dans l'eau. Des solutions cristallise ZnSO4 · 7H2O - sulfate de zinc. Utilisé dans la production de viscose, d'émaux, pour protéger le bois de la pourriture.
SULFATE DE ZINC
SULFATE DE ZINC (sulfate de zinc) Zinci sulfas, ZnSO4. ZnSO4 · 7H2O - le sulfate de zinc cristallise à partir des solutions. Utilisé dans la production de viscose, d'émaux, pour protéger le bois de la pourriture.
Caractéristique:
Cristaux transparents incolores ou poudre cristalline fine de goût astringent, inodore. Il s'érode dans l'air. Dissolvons très facilement dans l'eau, pratiquement insoluble dans l'éthanol, dissolvons lentement dans la glycérine (1:10). Les solutions aqueuses sont acides.
Le sulfate de zinc a des effets antimicrobiens, astringents, desséchants et anti-inflammatoires locaux.
Application:
Conjonctivite, laryngite, urétrite, vaginite - par voie topique; la nécessité de faire vomir - à l'intérieur à fortes doses; carence en zinc dans le corps avec troubles des processus anaboliques, immunologiques et autres (prévention et traitement) - à l'intérieur; hypogonadisme, alopécie areata, paralysie cérébrale, maladie du foie, diabète sucré, maladies diffuses du tissu conjonctif, etc. (dans le cadre d'une thérapie complexe) - à l'intérieur.
Contre-indications:
Hypersensibilité.
Effets secondaires:
Nausées, vomissements, diarrhée (lors de la prise de fortes doses par voie orale).
Sulfate de zinc, sulfate de zinc, ZnSO4 - sel de zinc de l'acide sulfurique.
Cristaux incolores, densité 3,74 g / cm³. Solubilité dans l'eau (%): 29,4 (0 ° C), 37,7 (99 ° C). ZnSO4 · 7H2O (sulfate de zinc) cristallise à partir de solutions à des températures inférieures à 38,8 ° C, ZnSO4 · 6H2O dans la gamme de 38,8 ° C à 70 ° C, ZnSO4 · H2O monohydrate se forme au-dessus de 70 ° C Ce dernier est déshydraté à 238 ° C. Le sulfate de zinc dans la gamme de 600-900 ° C se décompose en ZnO et SO3. Les solutions faibles de sulfate de zinc deviennent troubles pendant l'hydrolyse en raison de la précipitation de 3Zn (OH) 2 · ZnSO4 · 4H2O.
Recevoir
Le sulfate de zinc est obtenu par évaporation et cristallisation à partir de solutions (avec la production de zinc). Zn + H2SO4 \u003d ZnSO4 + H2
Application
Il est utilisé dans la production de viscose, de peintures minérales, d'émaux, en métallurgie (réactif de flottation) et en médecine.
Principe actif-actif / début: zinc (sulfate de zinc, picolinate, asparaginate)
Bio-zinc; Le picolinate de zinc Solgar; Sulfate de zinc; Asparaginate de zinc; Picolinate de zinc; Sulfate de zinc; Zincite; Zincteral.
Il est utilisé pour les maladies du foie (cirrhose), les entérites, la dermatite entéropathique, le psoriasis, les maladies du collagène (polyarthrite rhumatoïde, lupus érythémateux), la paralysie cérébrale, les rhumes fréquents. Il est utilisé localement pour la conjonctivite, la laryngite, l'urétrite, la vaginite.
Zinc (sulfate de zinc, picolinate, asparaginate).
Formes posologiques:
Comprimés effervescents.
Gouttes pour les yeux.
Solution à usage externe.
Zinc (sous forme de sulfate de zinc, picolinate, asparaginate)
Propriétés / Action:
Le zinc est un oligo-élément essentiel. Il fait partie intégrante de plus de 90 enzymes différentes qui effectuent la synthèse d'ADN et sont impliquées dans les processus métaboliques. Le zinc stimule la synthèse des acides nucléiques, des protéines, la régénération des tissus et aide à augmenter le poids corporel. Le zinc est essentiel au fonctionnement de l'insuline, hormones des gonades, maintient la stabilité des membranes cellulaires, limitant la libération d'histamine par les mastocytes. Il limite les réactions des radicaux libres, prévient les dommages aux membranes cellulaires. Le zinc est essentiel à l'activité normale du tissu lymphoïde, de la phosphatase alcaline, des carboxypeptidases et de l'alcool déshydrogénase.
Le zinc augmente la résistance aux maladies infectieuses, favorise la cicatrisation des plaies, accélère la croissance, augmente l'efficacité, améliore la mémoire et prévient la chute des cheveux.
Certaines populations, telles que les femmes enceintes, les mères allaitantes, les adolescents, les athlètes et les végétariens réguliers, ont un besoin accru de zinc. Une carence en zinc peut être causée par un apport insuffisant dans le corps ou une alimentation malsaine, une alimentation déséquilibrée, une absorption altérée du zinc (par exemple, avec des maladies intestinales) ou une augmentation de l'excrétion de zinc, par exemple, avec l'alcoolisme, la prise de laxatifs ou d'autres médicaments.
Les indications:
Élimination de l'hypocincémie, incl. avec des troubles des processus anaboliques, immunologiques et autres, pouvant survenir avec des maladies du foie (en particulier avec la cirrhose), la stéatorrhée, l'entérite, l'invasion helminthique, l'acrodermatite entéropathique, le psoriasis, les maladies rénales, l'hypovitaminose D, avec des brûlures.
En prophylaxie pour les affections suivantes: diabète sucré, collagénose (polyarthrite rhumatoïde, lupus érythémateux), hypogonadisme, alopécie areata, paralysie cérébrale, rhumes fréquents, prise de glucocorticoïdes, grossesse et allaitement.
Topiquement (sulfate de zinc):
Conjonctivite, laryngite, urétrite, vaginite.
Mode d'administration et posologie:
À jeun, sous forme de pilules ou de comprimés effervescents. Pour la prévention de l'hypocincémie, 10 mg de zinc 1 à 2 fois par jour. À des fins thérapeutiques - 20-50 mg 2-3 fois par jour.
Topiquement (sulfate de zinc):
Avec conjonctivite - collyre à 0,1-0,5%, avec laryngite - lubrification ou pulvérisation avec une solution à 0,25-0,5%, avec urétrite et vaginite - douche avec une solution à 0,1-0,5%.
Surdosage:
Ingestion possible: fièvre, dysfonctionnement pulmonaire, déshydratation, déséquilibre électrolytique plasmatique, léthargie, troubles des mouvements musculaires, insuffisance rénale.
Contre-indications:
processus auto-immuns actifs, en particulier l'encéphalite immunitaire;
insuffisance rénale aiguë, lésions rénales parenchymateuses sévères.
Application pendant la grossesse et l'allaitement:
L'application n'est possible qu'en cas de carence en zinc avérée dans le corps.
Effet secondaire:
Apparaît lors de la prise de fortes doses. Dans le même temps, des troubles dyspeptiques (nausées, vomissements, diarrhée), une déshydratation, un déséquilibre des électrolytes du plasma sanguin, une léthargie et une insuffisance rénale sont observés.
Lorsqu'elles sont utilisées à des doses thérapeutiques, les complications sont extrêmement rares.
Conditions de stockage:
À température ambiante, pas plus de 25 ° C.
Garder hors de la portée des enfants.
Les dates d'expiration sont indiquées sur l'emballage. Le médicament ne peut pas être utilisé après la date d'expiration.
Congé de pharmacie: sans ordonnance du médecin.
Oxyde de zinc (Zincioxidum)
Blanc ou blanc avec un éclat jaunâtre, poudre amorphe et inodore. Absorbe le dioxyde de carbone de l'air .
Pratiquement insoluble dans l'eau et l'alcool, soluble dans les solutions alcalines, les acides minéraux dilués et aussi dans l'acide acétique.
Lorsqu'elle est chauffée, la substance change de couleur: blanche à température ambiante, l'oxyde de zinc devient jaune. Ceci s'explique par une diminution de la bande interdite et un décalage des bords du spectre d'absorption de la région UV vers le bleu.
Oxyde de zinc amphotère - réagit avec les acides pour former des sels, lorsqu'il interagit avec des solutions alcalines forme des tri-tétra- et hexahydroxyzincates complexes (Na2, Ba2):
OH- 2-
L'oxyde de zinc se dissout dans une solution aqueuse d'ammoniaque, formant un complexe ammoniac:
ZnO + 4NH3 + Н20 - (OH) 2
Lorsqu'il est allié avec des alcalis et des oxydes métalliques, l'oxyde de zinc forme des zincates:
ZnO + 2NaOH Na2ZnO2 + H2O
ZnO + CoO CoZnO2
Lorsqu'il est allié aux oxydes de bore et de silicium, l'oxyde de zinc forme des borates et silicates vitreux:
ZnO + B2O3 Zn (BO2) 2
ZnO + SiO2 ZnSiO3
Recevoir
zincite minérale naturelle
combustion de vapeur de zinc dans l'oxygène ("procédé français")
décomposition thermique des composés:
acétate de Zn (CH3COO) 2
hydroxyde de Zn (OH) 2
carbonate ZnCO3
nitrate de Zn (NO3) 2
grillage oxydant du sulfure de ZnS
synthèse hydrothermale
l'extraction des poussières et des boues des usines métallurgiques, en particulier celles qui utilisent la ferraille comme matière première (elle contient une part importante de fer galvanisé).
extraction du triple système d'équilibre de phase "nitrate de zinc-nitrate d'amine-eau" (avec pyridine et nitrate de quinoléine, la taille des particules est d'environ 5-10 nm jusqu'à 75%)
Application
activateur de vulcanisation de certains caoutchoucs
agent de vulcanisation du caoutchouc chloroprène
catalyseur de synthèse de méthanol
pigment blanc dans la production de peintures et d'émaux (actuellement (2007) remplacé par du dioxyde de titane non toxique TiO2)
charge et pigment en production:
les plastiques
parfumerie et cosmétique
En médecine, sous forme de poudres et de pommades comme antiseptique.
additif à l'alimentation animale
dans la production de verre et de peintures à base de verre liquide
comme l'un des composants du convertisseur de rouille
On sait également que l'oxyde de zinc a une activité photocatalytique, qui est utilisé en pratique pour créer des surfaces autonettoyantes, des revêtements bactéricides pour murs et plafonds dans les hôpitaux, etc. L'oxyde de zinc n'est actuellement pas utilisé pour la purification photocatalytique de l'eau à l'échelle industrielle.
En outre, la poudre d'oxyde de zinc est un matériau prometteur comme milieu de travail pour les lasers à poudre. Une LED bleue a été créée à base d'oxyde de zinc. Les films minces et autres nanostructures à base d'oxyde de zinc peuvent être utilisés comme capteurs de gaz sensibles et biologiques.
Les propriétés de l'oxyde de zinc déterminent son utilisation répandue dans l'industrie pharmaceutique. L'oxyde de zinc a trouvé une large application dans la création de dentifrices et de ciments abrasifs en dentisterie thérapeutique, dans les crèmes de bronzage et les procédures cosmétiques, dans la production de câbles électriques, de cuir artificiel et de produits en caoutchouc. De plus, l'application est répandue dans les industries du pneumatique, des peintures et vernis, du raffinage du pétrole. L'oxyde de zinc est impliqué dans la production de verre et de céramique.
Les préparations d'oxyde de zinc sont des agents dermatotropes anti-inflammatoires à effet desséchant à usage externe. L'oxyde de zinc a également un effet absorbant, astringent et antiseptique; forme des albumines et dénature les protéines. Réduit les phénomènes d'exsudation, d'inflammation et d'irritation des tissus, forme une barrière protectrice contre les facteurs irritants. Adoucit la peau irritée. Il est utilisé comme remède contre l'eczéma (au stade aigu), la dermatite (dermatite des couches, la dermatite de contact), l'érythème fessier, la chaleur piquante, les escarres, les plaies superficielles, les coupures, les égratignures, les brûlures, les lésions cutanées ulcéreuses, l'herpès simplex, la streptodermie, les ulcères trophiques.
Substance active-active:
Oxyde de zinc / Oxyde de zinc.
Formes posologiques:
Liniment.
Oxyde de zinc
Propriétés / Action:
L'oxyde de zinc a un léger effet astringent et est utilisé comme agent protecteur contre l'eczéma et la desquamation de la peau.
Les indications:
intertrigo;
dermatite, incl. dermatite des couches (érythème fessier chez les nourrissons), dermatite de contact;
escarres;
blessures superficielles, coupures, égratignures;
brûlures (thermiques, solaires);
lésions cutanées ulcéreuses;
eczéma au stade aigu;
l'herpès simplex;
streptodermie;
ulcères trophiques.
Mode d'administration et posologie:
Les préparations d'oxyde de zinc sont utilisées en externe, sous forme de pommade, pâte, liniment.
Lavez et séchez la zone affectée. Appliquer sur une peau nettoyée et séchée.
Les préparations d'oxyde de zinc sont appliquées en couche mince sur la peau affectée 4 à 6 fois par jour.
Le cours du traitement dure jusqu'à 1 mois.
La quantité de médicament appliquée dépend de l'étendue de la lésion.
Petits coups de soleil et thermiques, coupures, égratignures, plaies - appliquez une fine couche sur la surface affectée, si nécessaire appliquez un bandage de gaze.
Éruption cutanée chez les enfants - si les premiers signes d'hyperémie, d'érythème fessier ou d'irritation mineure de la peau apparaissent, la pommade est appliquée 3 fois ou plus par jour, si nécessaire à chaque changement de couche; traité prophylactiquement avec les zones médicamenteuses du corps qui sont en contact à long terme avec du linge humide.
Contre-indications:
intolérance individuelle (y compris des antécédents d'hypersensibilité) à l'oxyde de zinc.
Effets secondaires:
Réactions allergiques (prurit, rougeurs, éruptions cutanées).
Instructions spéciales et précautions:
Seulement pour usage externe. Éviter le contact visuel.
La pommade est appliquée uniquement sur les lésions superficielles et non infectées et n'est pas utilisée pour traiter les lésions cutanées pustuleuses. Non destiné à prescrire un traitement sans la participation d'un médecin.
Le médicament n'est pas contre-indiqué pendant la grossesse et l'allaitement.
Interaction médicamenteuse:
Non décrit.
Conditions de stockage:
À des températures jusqu'à 30 ° C, loin des sources de chaleur et de la lumière directe du soleil.
La durée de conservation est indiquée sur l'emballage.
Quittez la pharmacie - sans prescription médicale.
Pendant des siècles, l'oxyde de zinc a été utilisé en médecine. Des mentions à son sujet se trouvent dans l'ancien texte médical indien "Charaka Samhita". En outre, l'utilisation de l'oxyde de zinc à des fins médicinales est décrite par le médecin grec Dioscoride. Aujourd'hui, cette substance trouve une variété d'applications à la fois en pharmacologie et dans l'industrie.
Oxyde de zinc Est un composé inorganique présent dans la croûte terrestre sous forme de minéral appelé zincite. Cependant, afin de répondre à l'essentiel de la demande commerciale de ce composé, il est également synthétisé artificiellement. La formule chimique de l'oxyde de zinc est ZnO. C'est une substance blanche et poudreuse qui ne se dissout pas dans l'eau et l'alcool, mais se dissout dans la plupart des acides, y compris l'acide chlorhydrique (HCl).
Brûler du zinc dans l'air pour produire de l'oxyde de zinc était une pratique courante chez les alchimistes. La substance qui en résulte semble très lâche et ressemble à des touffes blanches de laine, c'est pourquoi on l'appelle la «laine des philosophes».
Le zincite minéral peut être légèrement jaunâtre ou rosâtre en raison de la présence de manganèse et d'autres impuretés. On sait que l'oxyde de zinc réagit fortement avec la poudre d'aluminium et de magnésium. Une autre propriété intéressante de ce composé inorganique est qu'il est capable d'absorber le rayonnement ultraviolet. De plus, l'oxyde de zinc est connu pour ses propriétés telles qu'une conductivité thermique élevée et des propriétés antibactériennes.
L'utilisation de l'oxyde de zinc en médecine
- L'oxyde de zinc a des propriétés antibactériennes et est donc largement utilisé dans le traitement d'un certain nombre d'affections cutanées. Il est utilisé comme agent topique pour réduire les irritations cutanées et pour traiter les brûlures et coupures mineures. Il peut également être utilisé comme remède contre la peau sèche et gercée.
L'oxyde de zinc est utilisé dans les soins des nouveau-nés

L'oxyde de zinc est le produit le plus largement utilisé pour le traitement et la prévention de l'érythème fessier.
Il forme essentiellement une barrière protectrice entre la peau et la couche,
ainsi, empêchant l'apparition d'éventuelles éruptions cutanées.
- En raison de ses propriétés médicinales, il est ajouté aux poudres pour bébé, aux shampooings antipelliculaires, aux crèmes antiseptiques et aux bandes chirurgicales. Avec l'oxyde de fer, ce composé est utilisé pour créer un fluide contre les coups de soleil (lotion calamine).
- L'oxyde de zinc est mélangé avec de l'eugénol pour obtenir de l'oxyde de zinc avec de l'eugénol, qui est utilisé en dentisterie pour les prothèses et la restauration dentaire.
- Sa capacité à soulager les démangeaisons et les irritations cutanées fait de l'oxyde de zinc un ingrédient important dans de nombreux suppositoires rectaux utilisés pour soulager l'irritation et l'inconfort des hémorroïdes.
- En outre, cette substance sert de source de zinc nutritif minéral, qui est nécessaire pour un large éventail de réactions dans le corps. Par conséquent, il est ajouté à des compléments alimentaires ou vitaminiques. En tant que complément alimentaire, l'oxyde de zinc se trouve également dans les céréales pour petit-déjeuner enrichies en vitamines et minéraux. En raison de ses propriétés fongistatiques, il est utilisé dans la production de matériaux d'emballage pour la viande, le poisson et les légumes.
L'utilisation de l'oxyde de zinc en cosmétologie
- L'oxyde de zinc est capable d'absorber les rayons ultraviolets du soleil et de protéger ainsi la peau des coups de soleil et autres dommages causés par les rayons UV.

- L'oxyde de zinc est l'un des ingrédients les plus importants des cosmétiques minéraux. Puisque la peau ne l'absorbe pas, elle n'irrite personne. De plus, son utilisation ne conduit pas à l'acné et ne provoque pas d'allergies.
- Entre autres, l'oxyde de zinc est utilisé dans la fabrication de déodorants et de savons. Il aide à éliminer les odeurs corporelles désagréables et empêche la croissance des bactéries. L'oxyde de zinc apaise également la peau et la protège des irritants.
Cependant, des précautions doivent être prises lors de l'application topique de produits à base d'oxyde de zinc ou d'oxyde de zinc. Il ne doit pas être utilisé pour traiter des brûlures et des plaies graves. Il est important d'éviter de mettre de l'oxyde de zinc dans vos yeux et votre bouche. L'exposition aux vapeurs d'oxyde de zinc peut irriter les poumons et provoquer une «fièvre de fonderie», semblable aux symptômes de la grippe. Ainsi, l'inhalation de vapeur d'oxyde de zinc est dangereuse, tandis que l'oxyde de zinc lui-même n'est pas toxique.
L'oxyde de zinc dans les cosmétiques pour bébés... L'oxyde de zinc est un agent anti-inflammatoire qui a un effet astringent, desséchant, antiseptique et adsorbant. Lorsqu'il est appliqué sur la peau affectée, l'inflammation et l'irritation sont réduites et une protection contre les irritants se forme. Il est utilisé pour diverses formes de dermatite, y compris l'érythème fessier, la chaleur épineuse et l'érythème fessier chez les enfants. Il est utilisé dans le traitement des plaies superficielles, coupures, égratignures, brûlures (thermiques et solaires). Traite les lésions ulcéreuses, les ulcères trophiques, l'eczéma aigu, les escarres, l'herpès simplex et la streptodermie. C'est absolument sans danger pour la santé. Il est utilisé comme base pour les cosmétiques décoratifs. Il est largement utilisé dans les cosmétiques solaires pour enfants et dans.
Le zinc dans la nature
Le zinc se trouve le plus souvent dans la nature dans les composés. Son composé le plus célèbre et principal est l'oxyde de zinc.
OXYDE DE ZINC (oxyde de zinc) Le ZnO est une poudre cristalline incolore qui est insoluble dans l'eau, jaunit lorsqu'elle est chauffée et se sublime à une température de 18000 C.
Méthode de production: par combustion de vapeurs de zinc dans l'air, formées lors de la fusion du minerai. Pour obtenir un produit plus pur et plus blanc, des vapeurs de zinc préalablement purifié sont brûlées.
Solubilité: soluble dans l'ammoniaque, l'acide acétique, les acides inorganiques dilués et les solutions alcalines. Insoluble dans l'eau et l'éthanol.
Propriétés chimiques: a des propriétés amphotères, réagit avec tous les acides pour former des sels.
Compatibilité avec les ingrédients de la recette: bien compatible avec tous les ingrédients de la série de cosmétiques pour bébés.
À l'étranger, des qualités spéciales d'oxyde de zinc (blanc de zinc) sont fabriquées, dont la composition, la taille moyenne des particules et les propriétés physico-chimiques sont différentes.
La formulation des cosmétiques pour bébés Magic Herbs utilise de l'oxyde de zinc importé.
L'oxyde de zinc vendu sur les marchés internationaux est classé en quatre grades:
- Pharma - Cette marque est utilisée dans l'électronique et la médecine.
- Neige - cette marque est utilisée pour la fabrication de produits en caoutchouc industriels de haute qualité, d'additifs alimentaires, de céramiques et de produits chimiques.
- Green Seal - cette marque est utilisée dans la production de produits en caoutchouc, du verre et des industries chimiques.
- Sceau rouge - Utilisé dans l'industrie du pneu.
Dans l'industrie cosmétique, les marques Pharma et Neige sont utilisées. Ils ont une granulométrie optimale de 0 4 - 0 6 μm. Ces marques ne contiennent pas de charges ou d'agents qui empêchent le mottage et offrent la meilleure protection contre les rayons UVB et UVA.
Application de l'oxyde de zinc en médecine, produits pharmaceutiques
Il y a cinq mille ans, les anciens Égyptiens utilisaient une pommade au zinc pour guérir les blessures. Il y a 100 ans, les scientifiques ont prouvé que le zinc est un élément essentiel pour les plantes et les humains.
Le zinc est impliqué dans la synthèse du collagène, élément vital pour la cicatrisation et la réparation des tissus cellulaires.
L'oxyde de zinc est largement utilisé en médecine en raison de son puissant effet anti-inflammatoire sur diverses infections cutanées. Le médicament est appelé blanc de zinc.
L'oxyde de zinc a la capacité d'attirer l'eau. En conséquence, les pommades à base de celle-ci gardent la plaie sèche, désinfectent et ont un léger effet astringent.
Les pommades au zinc sont efficaces pour les callosités et les fissures superficielles des jambes. L'oxyde de zinc est utilisé dans les imprégnations des plâtres médicaux.
Pour l'érythème fessier chez les enfants, des préparations d'oxyde de zinc sont utilisées, qui empêchent l'urine et d'autres irritants d'agir sur la peau, et adoucissent également la peau irritée et enflammée.
L'oxyde de zinc a un faible effet astringent et bactéricide. Il fait partie des produits à effet protecteur contre l'eczéma et le peeling cutané.
L'oxyde de zinc est impliqué dans de nombreux processus cellulaires, répare les tissus cellulaires endommagés, forme des albumines (composés de protéines de zinc) et dénature les protéines.
C'est le principal ingrédient actif des formes galéniques molles telles que la pâte de zinc, la pâte salicylique-zinc de Lassar, la pommade de Teimurov, ainsi que divers suppositoires.
Il est inclus dans la formulation de préparations pour peaux grasses et à problèmes. Il a des propriétés de raffermissement de la peau, resserre les pores de la peau et aide à éliminer l'acné.
L'utilisation de l'oxyde de zinc en cosmétologie et en cosmétique pour enfants.
L'oxyde de zinc est utilisé comme base pour la fabrication de divers produits cosmétiques décoratifs et crèmes pour le soin des peaux sensibles, grasses et à problèmes. Il est largement utilisé dans la fabrication de produits cosmétiques pour adolescents et enfants.
Les crèmes à l'oxyde de zinc créent une barrière protectrice entre la peau à problèmes et l'environnement, en plus d'hydrater et de nourrir la peau, de masquer ses imperfections et de la protéger du soleil.
L'oxyde de zinc est ajouté aux déodorants antisudorifiques solides pour son action antimicrobienne et sa capacité à empêcher la décomposition de la sueur. Les substances résultant de la décomposition de la sueur, comme l'acide butyrique, ont une odeur très désagréable. L'oxyde de zinc réagit avec ces acides gras. À la suite de la réaction, il se forme des produits qui n'ont plus d'odeur.
Les crèmes spéciales pour bébé qui protègent la peau délicate de bébé du dessèchement et de l'irritation par temps froid et venteux contiennent de l'oxyde de zinc.
L'oxyde de zinc est utilisé dans les écrans solaires comme filtre UV minéral. Étant donné que la crème solaire pour enfants doit contenir une protection non seulement contre les UVB, mais également contre les rayons UVA, l'oxyde de zinc est le filtre optimal pour les cosmétiques solaires pour enfants. L'oxyde de zinc, qui fait partie des écrans solaires avec un facteur de protection élevé de 15 et plus, prévient et protège la peau de l'enfant des zones ouvertes de la peau contre les brûlures, les irritations et les rougeurs.
Dans la série, l'oxyde de zinc est inclus dans les produits suivants.